Żadne treści nie pasują do wyszukiwanego hasła.
Wszystko
You have successfully logged out.
Rozporządzenie w sprawie wyrobów medycznych
Nowe europejskie rozporządzenie w sprawie wyrobów medycznych (MDR) z wieloma nowymi przepisami stanowi wyzwanie dla wszystkich zainteresowanych stron. B. Braun intensywnie przygotowuje się i chce jak najszybciej zastosować nowe wymagania. Tutaj zebraliśmy dla Ciebie kilka informacji na temat rozporządzenia MDR.
Zgodnie z obowiązującymi przepisami prawa, oświadczam, że jestem osobą wykonującą zawód medyczny lub prowadzącym obrót wyrobami medycznymi. Mam świadomość, że treści zamieszczane na niniejszej stronie mogą zawierać między innymi wiadomości na temat wyrobów niebezpiecznych dla zdrowia i bezpieczeństwa pacjentów.
Potwierdź Jestem profesjonalistą z branży medycznej. Anuluj Nie jestem profesjonalistą z branży medycznej.Nowe europejskie rozporządzenie w sprawie wyrobów medycznych (MDR) weszło w życie w maju 2017 r. Nowe rozporządzenie zastępuje istniejącą dyrektywę dotyczącą wyrobów medycznych (MDD) oraz dyrektywę dotyczącą aktywnych wszczepialnych wyrobów medycznych (AIMDD).
Prąd ok. 500 000 wyrobów medycznych w Europie zostanie ponownie certyfikowanych zgodnie z nową, znacznie bardziej kompleksową polityką w celu uzyskania znaku CE. Według aktualnych szacunków tylko około 65 procent wyrobów medycznych będzie certyfikowanych zgodnie z nowym rozporządzeniem. Niektóre jednostki notyfikowane są jeszcze w fazie wyznaczania i nie jest w pełni jasne, ile jednostek notyfikowanych będzie w stanie zakończyć proces ( lista na stronie internetowej Komisji Europejskiej ). Ze względu na zwiększone wymagania stawiane jednostkom notyfikowanym i producentom należy się spodziewać korekt portfela, których nie da się uniknąć.
Dotyczy to między innymi następujących obszarów:
Aby zapewnić ciągłe dostarczanie bezpiecznej i innowacyjnej technologii medycznej, wszyscy producenci muszą sprostać zwiększonym wymaganiom dotyczącym uzyskania znaku CE. Jednostki notyfikowane muszą położyć podstawy i stworzyć wystarczającą zdolność do przeprowadzenia procedury oceny zgodności.
Wcześniej firma B. Braun rozpoczęła już szeroko zakrojone przygotowania do certyfikacji własnych wyrobów medycznych zgodnie z rozporządzeniem MDR. Dotyczy to oczywiście wszystkich produktów, które firma B. Braun produkuje samodzielnie lub kupuje jako towary handlowe w celu uzupełnienia swojego portfolio. Jeśli chodzi o postęp podjętych środków, firma B. Braun ma pewność, że będzie w stanie spełnić wymagania rozporządzenia MDR do maja 2024 r.
Na szczeblu europejskim stała się konieczna zmiana dyrektywy w sprawie wyrobów medycznych 93/42 EWG (MDD), która została opublikowana w 1993 roku i nadal obowiązuje. Wraz z nowym rozporządzeniem władze UE chcą poprawić jakość wyrobów medycznych i zwiększyć bezpieczeństwo, zharmonizować procesy w UE i zwiększyć bezpieczeństwo pacjentów. Dodatkowe aspekty obejmują poprawę przejrzystości i identyfikowalności w połączeniu z nowymi technologiami, które umożliwiają jednoznaczną identyfikację wszystkich produktów w całym cyklu ich życia.
Rozporządzenie MDR określa wymagania, które producent musi spełnić, aby móc sprzedawać wyroby medyczne w Europie. Dotyczy to zarówno wymagań technicznych dotyczących produktu, jak i wymagań dotyczących monitorowania produktów stosowanych w placówkach opieki zdrowotnej.
Nastąpiło kilka zmian dotyczących klasyfikacji produktów. Oprócz wprowadzenia nowej klasy lr dla instrumentów chirurgicznych wielokrotnego użytku zwiększono wymagania stawiane produktom do implantacji klasy IIb. Ponadto liczne kategorie produktów zostały przypisane do wyższej klasy ryzyka. Rozporządzenie MDR zwiększa wymagania dotyczące dowodów klinicznych dotyczących wyrobów medycznych. W przyszłości wszystkie wyroby medyczne, niezależnie od ich klasy ryzyka, będą wymagać oceny klinicznej. Nowo wprowadzona procedura kontroli oznacza lepsze monitorowanie nowych, wszczepialnych produktów klasy ryzyka III, jak również aktywnych wyrobów medycznych, które podają i/lub usuwają leki klasy IIb przed wprowadzeniem na rynek. Oprócz zwiększonych wymagań stawianych producentom, obowiązują obecnie bardziej rygorystyczne przepisy dotyczące jednostek notyfikowanych. Aby móc zatwierdzić wyroby medyczne, muszą być spełnione różne dodatkowe wymagania. Jednostki notyfikowane są również zobowiązane do przeprowadzania niezapowiedzianych audytów u producentów. Dodatkowe wymagania dotyczące dokumentacji technicznej, które muszą być dostarczone przez producentów, znacznie zwiększają zakres i złożoność dokumentacji.
Na produkcie nie ma dokładnego identyfikatora wskazującego zgodność z rozporządzeniem MDR. Mimo to wraz z wprowadzeniem rozporządzenia MDR na etykiecie zostanie umieszczony nowy symbol ISO „MD” dla wyrobów medycznych.
Tak, dotyczy to wszystkich urządzeń medycznych wszystkich klas ryzyka, w tym jednostek i systemów terapeutycznych.
Dane istotne dla społeczeństwa są udostępniane w centralnej europejskiej bazie danych, która już istnieje. Rozszerzona wersja EUDAMED będzie wprowadzana stopniowo, tzn. dobrowolne wykorzystanie wersji „minimal viable product” (MVP) w 2022 r. Obowiązkowe stosowanie EUDAMED spodziewane jest w 2. kwartale 2025 r. Patrz oś czasu EUDAMED
Legalni producenci, producenci systemów i zestawów zabiegowych, importerzy lub upoważnieni przedstawiciele ds. dystrybucji wyrobów medycznych w UE muszą uzupełniać EUDAMED o dane dotyczące roli podmiotu, a także o dane dotyczące produktu dla każdego indywidualnego produktu, który ma być dystrybuowany w UE.
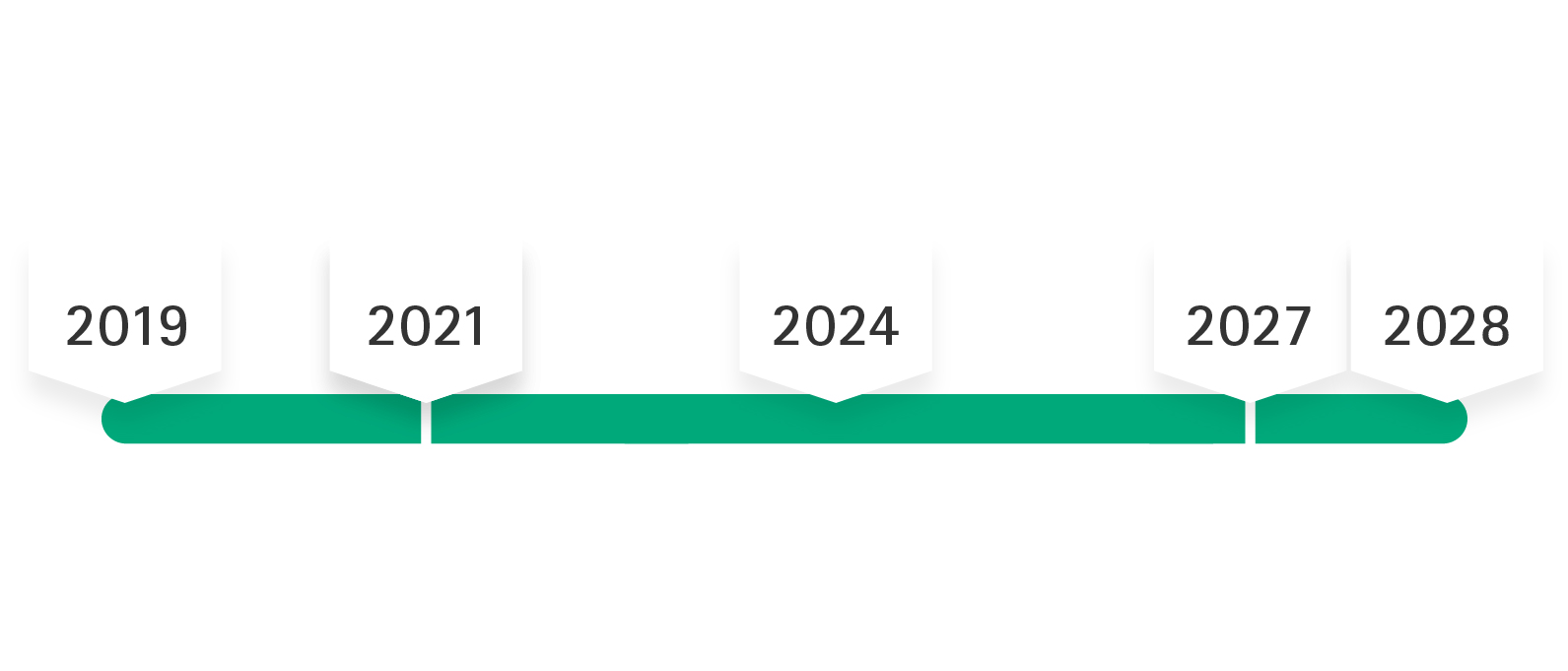
Po opublikowaniu rozporządzenia MDR 5 maja 2017 r. rozporządzenie weszło w życie 25 maja 2017 r., z okresem przejściowym, który miał trwać do 26 maja 2020 r. Ze względu na pandemię COVID-19 obowiązkowe stosowanie rozporządzenia MDR zostało odroczone do maja 2021 r. Zgodnie z 2. poprawką do rozporządzenia MDR czas przejściowy jest wydłużony do maks. grudzień 2028 r., tj. Certyfikaty MDD zachowują swoją ważność (tj. Maksymalny grudnia 2027 r. w przypadku produktów klasy ryzyka IIb wszczepialnych i III), jeśli spełnione są określone warunki wstępne.
Wyroby medyczne nie mogą stanowić niedopuszczalnego ryzyka dla zdrowia i bezpieczeństwa.
System QMS musi być już zgodny z rozporządzeniem MDR.
Wniosek MDR zostanie podpisany do maja 2024 r.
Umowa MDR z jednostką notyfikowaną zostanie podpisana do września 2024 r.
brak istotnych zmian w produktach MDD.
Zgodnie z 2. poprawką do MDR nie ma już ostatecznego okresu wyprzedaży. Wcześniej planowany okres wyprzedaży (tj. brak dalszej dystrybucji produktów z certyfikatem MDD po maju 2025 r.) został anulowany.
Ważność certyfikatu MDD EC została automatycznie przedłużona (nie są wystawiane nowe certyfikaty).
Certyfikaty MDD i MDR WE będą ważne równolegle w okresie przedłużenia osi czasu.
Produkty MDD i MDR mogą być wprowadzane na rynek równolegle.
Ze względu na pandemię COVID-19 obowiązkowy wniosek dotyczący rozporządzenia MDR został ustanowiony na 26 maja 2021 r. Wynikają z tego następujące terminy wprowadzenia na rynek wyrobów medycznych według klas produktów:
Klasa I: 26 maja 2021
Klasa Ir, s, m, Klasa IIa, Klasa IIb i Klasa III: 26 maja 2024 r.
Ocena zgodności określa, czy produkt i jego producent spełniają wymagania europejskiego rozporządzenia MDR. W zależności od klasyfikacji ryzyka poszczególnych produktów firma B. Braun jest uprawniona do samodzielnego przeprowadzenia tego audytu. Dodatkowe oceny są przeprowadzane przez tak zwaną jednostkę notyfikowaną.
Jednostka notyfikowana to prywatna firma wyznaczona w imieniu Unii Europejskiej do oceny zgodności producenta z rozporządzeniem MDR. Obecnie są one oceniane w ramach audytów, a po pomyślnym zaliczeniu audytów jednostki notyfikowane ocenią procesy producentów wyrobów medycznych pod kątem zgodności z rozporządzeniem MDR. Po zweryfikowaniu zgodności procesów przetwarzane produkty mogą zostać zarejestrowane w ramach tych procesów.
Nawet po przejściu całego portfolio produktów na rozporządzenie MDR producenci ponoszą znaczne dodatkowe koszty ze względu na zwiększone wymagania rozporządzenia MDR.
Głównymi celami rozporządzenia są lepsza ochrona zdrowia publicznego i bezpieczeństwa pacjentów, większa przejrzystość, bezpieczeństwo prawne i bardziej europejska koncepcja. Należy to osiągnąć poprzez szerszą dokumentację techniczną produktów, których dotyczy problem, w systemie zarządzania jakością zgodnym z MDR.
Jako producent wyrobów medycznych firma B. Braun musi spełniać wymagania rozporządzenia MDR. Różne grupy robocze aktualizują dokumentację techniczną i przeglądają procesy, aby zapewnić zgodność z rozporządzeniem MDR. Ponadto firma B. Braun jest zobowiązana do udostępniania EUDAMED informacji o produkcie, w tym unikalnych danych identyfikacyjnych wyrobu (UDI), a także informacji dotyczących nadzoru po wprowadzeniu na rynek.
Grupa B. Braun zainicjowała kompleksowe działania i udostępniła zasoby w celu zapewnienia terminowego wdrożenia rozporządzenia MDR.
Wszystkie wyroby medyczne
Firma B. Braun od jakiegoś czasu intensywnie przygotowuje się do nowych przepisów i zakłada, że będzie w stanie dotrzymać harmonogramu.
Systemy zarządzania jakością firmy B. Braun Melsungen AG, B. Braun Avitum AG i Aesculap AG zostały już certyfikowane zgodnie z rozporządzeniem MDR i przygotowano już dokumentację techniczną zgodną z rozporządzeniem MDR dla naszych produktów. Przeniesienie produktu do rozporządzenia MDR będzie odbywać się sukcesywnie do maksymalnego okresu.
Zasadniczo tak - w zależności od planowanego cyklu życia produkty są certyfikowane zgodnie z MDR. Podobnie jak w poprzednich latach, B. Braun będzie nadal dostosowywał swoje portfolio produktów. Do portfolio zostaną dodane nowe produkty, a starsze generacje zostaną zastąpione lub nieekonomiczne lub przestarzałe produkty zostaną usunięte z portfolio produktów. W ramach naszego regularnego procesu zarządzania asortymentem będziemy nadal informować odpowiednich klientów o odpowiednich zmianach w asortymencie produktów w sposób terminowy, otwarty, przejrzysty i ukierunkowany oraz w miarę możliwości oferować alternatywy.
B. Braun korzysta z okresu przejściowego MDR, w którym przeniesiemy naszą ofertę produktów do MDR. W tym okresie przejściowym firma B. Braun wprowadzi na rynek zarówno produkty z certyfikatem MDD, jak i MDR.
W maju 2019 roku TÜV Süd został uznany za drugą jednostkę notyfikowaną na świecie. Inne jednostki notyfikowane nadzorujące wyroby medyczne firmy B. Braun to MedCert, Dekra i TÜV Rheinland, które zostały również wyznaczone zgodnie z rozporządzeniem MDR. Aby uzyskać przegląd akredytowanych jednostek notyfikowanych MDR, proszę zapoznać się z linkiem do strony internetowej Komisji Europejskiej.
Strona Komisji Europejskiej
a) Identyfikacja wyrobu medycznego ulegnie zmianie poprzez dodanie unikalnego identyfikatora wyrobu (UDI).
b) W przypadku nowych produktów klasy III mogą wystąpić rozszerzone obowiązki dokumentacji.
c) Baza danych EUDAMED zapewnia klientom większą przejrzystość w zakresie produktów.
Firma B. Braun jest gotowa do stosowania rozporządzenia MDR i w tym celu już zainwestowała w wielocyfrowy milionowy zakres. Głównymi czynnikami kosztowymi są bardziej kompleksowe wymagania dotyczące dokumentacji technicznej, rozwiązania techniczne i systemowe w celu spełnienia wymagań dotyczących zarządzania danymi EUDAMED, a także zwiększone wysiłki w zakresie nadzoru po wprowadzeniu na rynek.
Firma B. Braun aktywnie wspiera klientów w uzyskiwaniu informacji. W tym celu deklaracje zgodności i informacje dotyczące użytkowania (IFU) są sukcesywnie udostępniane w formie cyfrowej od maja 2021 r.
Deklaracje zgodności można znaleźć na stronie internetowej www.bbraun.com - po prostu wpisując nazwę produktu w polu wyszukiwania i wyszukując odpowiednią deklarację zgodności w rubryce -powiązane dokumenty-. Większość deklaracji zgodności B. Braun Melsungen AG i B. Braun Avitum AG jest dostępna za pośrednictwem tego kanału. Ze względów technicznych firma B. Braun będzie mogła udostępniać deklaracje zgodności produktów Aesculap AG (z wyjątkiem portfolio materiałów nici chirurgicznych) online tylko w średnim terminie. W celu losowego udostępnienia deklaracji zgodności, których nie można znaleźć w Internecie, należy skontaktować się ze znanym działem obsługi klienta krajowej spółki-córki B. Braun.
Instrukcję obsługi można pobrać ze strony https://eifu.bbraun.com Po wprowadzeniu numeru artykułu lub GTIN wyświetlane są dokumenty przynależne do produktu.
Oto zbiór przydatnych linków do informacji na oficjalnych stronach internetowych Komisji Europejskiej i innych źródłach.
Arkusz informacyjny dla pracowników służby zdrowia (strona internetowa UE)
link
Dziennik EU: Rozporządzenie w sprawie wyrobów medycznych
link
Lista jednostek notyfikowanych (UE)
link
Harmonogram EUDAMED (UE)
link
Elektroniczna instrukcja użytkowania (eIFU) firmy B. Braun
link
Arkusz informacyjny B. Braun dotyczący rozporządzenia MDR
pdf, 53.6 KB
Pytania i odpowiedzi dotyczące praktycznych aspektów przepisów przejściowych MDR
link
Spersonalizowane konto sprawia, że korzystanie z Internetu jest łatwiejsze, wygodniejsze i bezpieczniejsze.